-
-
輔導深圳某企業獲呼吸機NMPA注冊證
2024-10-18
文章出處:成功案例 網責任編輯: 醫療器械全球注冊服務/體系認證/臨床試驗代理-瑞恩尼咨詢 閱讀量:1549 發表時間:2024-07-17
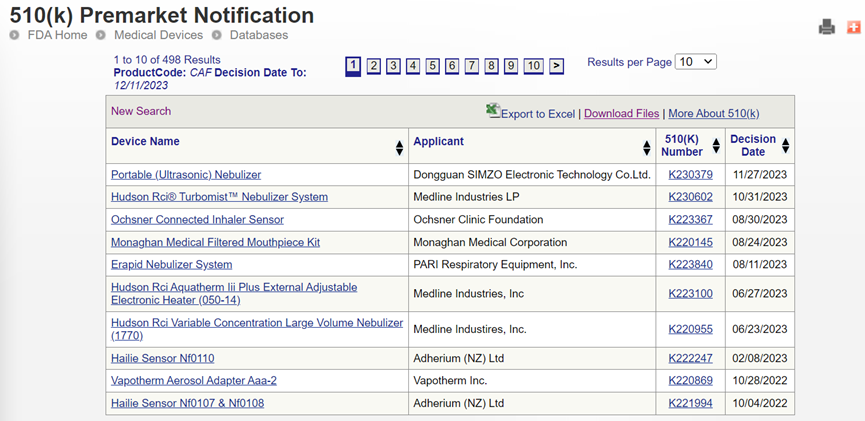
瑞恩尼助力東莞某企業獲得超聲霧化器FDA 510k注冊
在2023年2月,瑞恩尼提交了一款霧化器510(k)申請,經過努力終于在11月底通過FDA審核,取得美國上市資質。縱貫近年來FDA審批通過的霧化器記錄,確實屈指可數,整個呼吸治療類系列的產品,都得到了FDA的特別關注,審評尺度非常嚴格,也難各咨詢業與制造商特別難受。
下面簡略地分享一下在申請過程中遇到的問題和經驗。
1. 510k適用標準:
序號 | 類別 | 標準號 |
1 | 電氣安全 | IEC 60601-1 |
2 | 電磁兼容 | IEC 60601-1-2 |
3 | 軟件 | IEC 62304 |
4 | 家用電氣安全 | IEC 60601-1-11 |
5 | 風險 | ISO 14971& ISO TR24971 |
6 | 生物相容性 | ISO 10993系列標準(根據實際測試項目而定) |
7 | 氣路生物相容性 | ISO 18562-1/-2/-3 |
8 | 清潔/消毒 | FDA 醫療器械重復處理指南及相應標準 |
9 | 顆粒特性 | FDA霧化器指南,美國藥典 |
10 | 性能標準 | ISO 27427 |
2. 生物相容性要求
基于霧化器是將藥物霧化,通過呼吸進入呼吸道或肺部沉積,藥杯,面罩,軟管等藥物通路的生物相容性分類為永久(>30天)與組織接觸的外部接入器械。因此,其生物相容性要求較高,除了基本三項之外,還需要根據ISO 10993-1 表A.1的要求進行更多的生物相容性測試。或者采用化學表征及毒理學評估代替部分測試,如慢性毒性和遺傳毒性。其中化學表征的測試需特別注意達到窮盡提取,并在有機化合物的分析過程中,選擇多種標準物質進行定量分析。
3. 呼吸氣路生物相容性要求
霧化器還存在氣體通路,因此還需結合實際情況進行ISO 18562系列標準的測試。在做這些測試的過程中,主要問題是測試條件、測試方法要清晰,完整,結果應盡量詳細,如VOC的測試應保證達到穩定狀態或低于容許攝入量,并在測試過程中考慮預期壽命內最壞情況的暴露。
4. 霧化顆粒特性
霧化器的氣霧性能測試也是FDA關注的重點,依據FDA關于霧化器審評指導原則的要求,至少包含與3種藥物的霧化粒徑分布測試。FDA認可的霧化顆粒測試為多級聯撞擊測試法,這與我們在國內普遍測試使用的激光散射法不同。目前在國內很少有實驗室有測試設備、方法與與FDA應審的經驗,所以實驗室的選擇非常重要。
5. 壽命特性
霧化器的壽命期限對于霧化顆粒的影響,對于清潔消毒的影響也是FDA會關注到的方面。過往大家都容易在做出樣機后,通過驗證來證明產品的符合性。可是這種做法,往往只能證明產品符合相應驗證要求,但是無法證明在產品的整個生命周期內,產品都是符合相應的驗證要求的。
最后總結一下,對于一些FDA關注度高的醫療器械,FDA對于檢測報告的要求非常高,選擇有成功經驗有豐富技術經驗的實驗室將非常重要。隨著FDA的審核日趨嚴格,現在審核已經從以往產品描述性資料,精度大量過度到驗證和確認報告上面。所以如在國內注冊與CE注冊中養成的,只要找實驗室出了報告就沒有問題的時代已經過去了。
同樣,選擇一個有同產品經驗的咨詢公司,也是項目成功的非常重要的一個因素。瑞恩尼咨詢完成了一次性霧化器,壓縮霧化器、超聲霧化器與網式霧化器數十個案例的國內,CE與FDA的項目。對于霧化器的特性積累了非常豐富的實戰經驗,同時部分咨詢師也在霧化器行業的企業工作過。這些經驗將有助于瑞恩尼能更好地為霧化器的企業提供咨詢服務。
