-
-
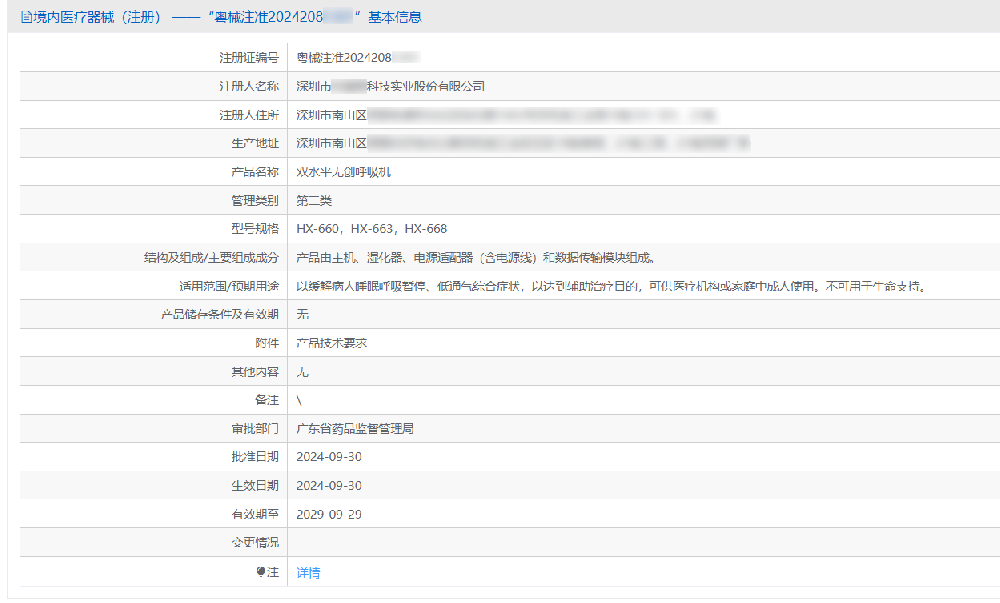
輔導深圳某企業獲呼吸機NMPA注冊證
2024-10-18
文章出處:成功案例 網責任編輯: 醫療器械全球注冊服務/體系認證/臨床試驗代理-瑞恩尼咨詢 閱讀量:325 發表時間:2024-06-19
2021年9月2日,由深圳市醫療器械質量管理促進會舉辦為期2天的 “美國QSR 820體系與510K注冊專題培訓”,在邁瑞公司報告廳圓滿落幕。
本次專題培訓由深圳市醫療器械質量管理促進會與深圳市瑞恩尼醫療器械管理咨詢有限公司聯合承辦,瑞恩尼王海龍總經理主講!
隨著我國醫療器械產業的不斷發展和壯大,醫療器械企業邁出國門,產品走向世界市場勢在必行。美國是醫療器械產品的大市場之一,FDA是對醫療器械監管具有經驗的監管機構,其法規體系的要求也是非常嚴格和詳盡。為幫助意向開拓美國市場的醫療器械企業,為其醫療器械產品在美國銷售獲得通行證,促進會聘請具有多年FDA工廠檢查案例和FDA 510K注冊及企業注冊、登記列名案例經驗的行業專家講授QSR 820體系建立和有效運行及510K注冊知識,旨在幫助醫療器械企業提高醫療器械產品在FDA注冊的成功率和質量管理體系的規范運行。
本次培訓內容豐富,實用性和針對性強,主要包括:FDA醫療器械監管法規體系、21 CFR 820與ISO 13485的差異、FDA工廠檢查、21 CFR QSR 820質量體系法規、21 CFR 801 標簽、21 CFR 807 醫療器械制造商和進口商的企業登記及產品列名、21 CFR 830 UDI、21 CFR 860 醫療器械分類程序、510K注冊等。
本次培訓,得到了會長單位深圳邁瑞生物醫療電子股份有限公司的大力支持!促進會以感恩、回饋的之心,誠邀了60余家陪伴、支持促進會成長5年以上的會員企業免費參加培訓,現場參加培訓的人員按疫情防控要求佩戴口罩、分開就坐。培訓過程進行了互動答疑,學員們就QSR820質量管理體系和510K注冊問題積極踴躍地向老師進行咨詢,老師逐一給予解答,學員對本次專題培訓內容興趣濃厚、對本次培訓學習給予高度贊譽。
